Paradoxul cercetării în domeniul oncologic
Paradoxul cercetării în domeniul oncologic este reprezentat de faptul că pe măsură ce cunoștințele noastre despre această boală sporesc, în aceeași măsură recunoaștem din ce în ce mai mult complexitatea acestei patologii.
Timp de secole, am numit cancerul conform organului afectat inițial; însă progresele extraordinare realizate în materie de profil genetic au permis identificarea a mai multor subtipuri, fiecare cu propriile profiluri moleculare și prin consecință, propriile profile de prognostic. De exemplu, acum se știe despre cancerul pulmonar că nu este o singură boală, ci cuprinde peste zece subtipuri diferite, toate determinate de diferite căi moleculare.1 Această înțelegere a permis începerea dezvoltării unor tratamente care țintesc în mod specific mecanismele moleculare, care conduc la apariția diferitelor tipuri de cancer, declanșând o eră a medicinei personalizate în care o abordare generală nu mai este răspunsul.
Trecerea la îngrijirea medicală personalizată a contribuit la îmbunătățiri globale în ceea ce privește ratele de supraviețuire ale cancerelor. În Europa, numărul cazurilor de deces cauzate de cancer a scăzut cu aproximativ 10% de la finalul anilor 1980,2 în vreme ce în prezent numeroși pacienți diagnosticați cu cancer au speranță de viață de peste 10 ani.3,4
Aceste tendințe sunt încurajatoare pentru a putea livra în continuare terapii inovatoare pacienților care au nevoie de ele, motiv pentru care și modul de evaluare a noilor medicamente trebuie să evolueze și să țină pasul cu nivelul crescut de înțelegere în ceea ce privește biologia cancerului.
Obiective urmărite în studiile clinice
Supraviețuirea globală (OS) este intervalul de timp în care o persoană cu cancer supraviețuiește după începerea tratamentului. Este o unitate de măsură care a fost utilizată în studiile clinice de mai multe decenii și care rămâne standardul de aur pentru stabilirea eficacității unui medicament. Pe măsură ce persoanele care suferă de cancer au o speranță de viață mai mare, poate fi nevoie de mai mult timp și resurse pentru a demonstra dacă un medicament nou îmbunătățește în mod semnificativ perioada de supraviețuire comparativ cu o terapie mai veche. Mai mult, pacienții cu cancer din prezent vor beneficia de o serie de tratamente consecutive pe parcursul bolii lor, ceea ce înseamnă că este dificil de determinat eficacitatea pe termen lung a unui anumit medicament care a fost administrat în cadrul unui studiu clinic.5
Pentru a depăși aceste abordări nepractice, au fost introduse criterii precum rata de supraviețuire fără progresia bolii (PFS)* și rata de răspuns global (ORR)**.
Aceste criterii erau necunoscute în urmă cu 30 de ani, dar în prezent sunt utilizate frecvent în studii clinice și sunt acceptate pe scară largă de către autoritățile de reglementare ca surogate pentru OS.6
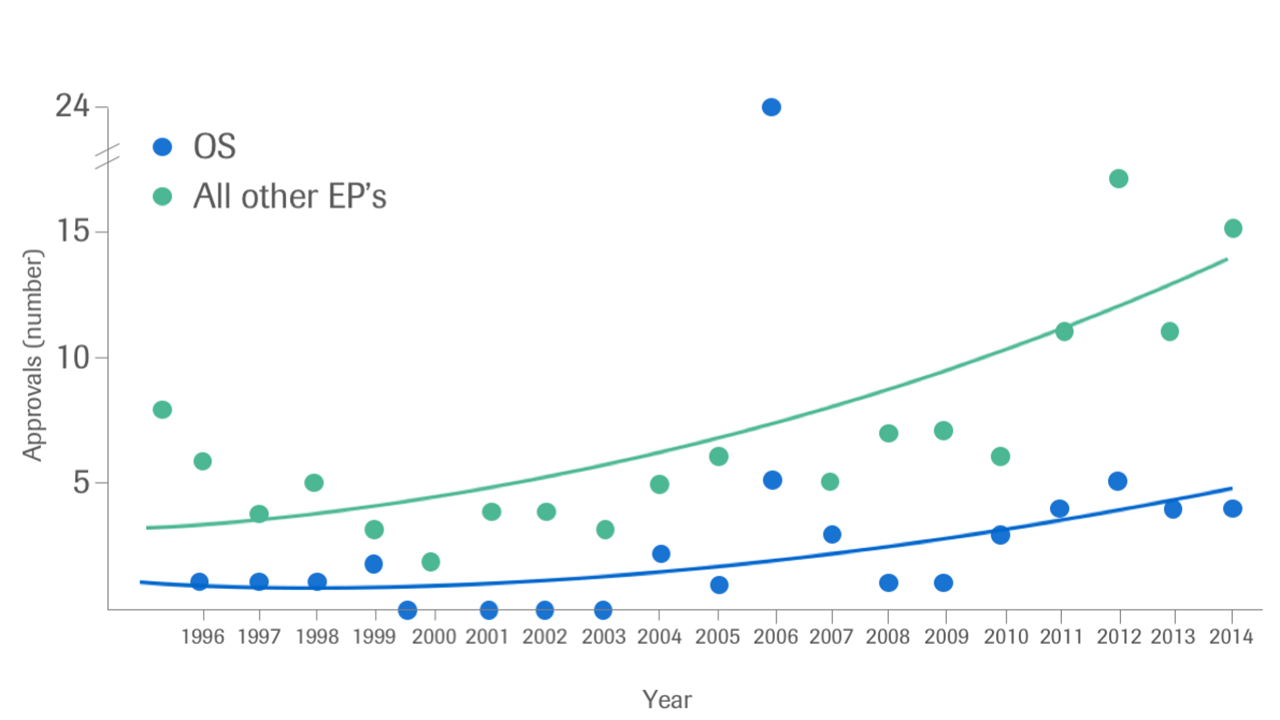
Figura 1: Reprezentare grafică a numărului de aprobări FDA, 1996 – 2004, în funcție de rata de supraviețuire globală ca criteriu comparativ cu alte criterii utilizate în studiile clinice7
Epoca modernă a criteriilor de evaluare în studiile clinice
Recent, dezvoltarea tehnologiilor de imagistică extrem de precise au permis explorarea de metode mai noi și mai specifice bolilor de măsurare a răspunsului unei tumori la tratament.
De exemplu, în cazul malignităților hematologice, boala minimă reziduală (minimal residual disease - MRD) este o afecțiune în care un număr redus de celule canceroase rămân în fluxul sanguin sau în măduva osoasă a pacienților după administrarea tratamentului. Obținerea unui status ‘MRD negativ’ înseamnă că un pacient se află în remisie profundă și nu mai se mai detectează celule canceroase, chiar și după efectuarea unor teste moderne și mai precise.8
În mod similar, în cazul cancerului mamar incipient, răspunsul patologic complet (pCR) poate fi utilizat pentru a evalua eficacitatea unui medicament administrat înainte de intervenția chirurgicală (în secvența neoadjuvantă). Obținerea unui pCR înseamnă că nu mai sunt detectate celule canceroase la momentul intervenției chirurgicale la nivelul sânului afectat și a ganglionilor limfatici. pCR poate fi măsurat mai rapid decât criteriile tradiționale, unele studii sugerând asocierea acestuia cu îmbunătățirea, înregistrate în rezultatele pe termen lung.8
Pe măsură ce știința în continuă evoluție provoacă identificare de metode inovatoare de măsurare a eficacității clinice a tratamentelor oncologice, modul în care înțelegem criteriile deja stabilite se schimbă, de asemenea. De exemplu, rata de supraviețuire fără semne de boală (DFS***) a fost recunoscută timp de mai multe decenii ca surogat pentru OS în studiile privind cancerul mamar incipient. Cu toate acestea, în ultimii ani, investigatorii au utilizat la scară amplă o versiune adaptată a acestui criteriu, cunoscută ca rata de supraviețuire fără boală invazivă (iDFS****), în special în cadrul unui tratament adjuvant împotriva cancerului mamar. Acest criteriu este adesea preferat întrucât permite o estimare mai clară a efectului tratamentului asupra bolii.
Măsurarea răspunsului imunoterapiei, o nouă clasă de medicamente, presupune o abordare cu totul diferită. În numeroase cazuri, recrutarea sistemului imunitar să atace o tumoră generează o creștere aparentă a dimensiunii tumorii într-un stadiu incipient, urmată de o micșorare dramatică și durabilă datorită naturii dinamice a sistemului imunitar. Astfel, a fost dezvoltat un nou set de criterii, cunoscute drept criteriile privind răspunsul imun (irRC) pentru a colecta mai bine modelele de răspuns observate la anumite imunoterapii, ceea ce permite o evaluare mai cuprinzătoare a impactului lor.
Măsurarea indicilor care contează
Pe lângă extinderea vieții, tratamentele trebuie să și susțină sau să îmbunătățească calitatea vieții pacienților (QoL). QoL este măsurată cu ajutorul rezultatelor raportate de pacienți (PROs) care sunt colectate prin intermediul sondajelor și care acoperă aspecte diverse despre bunăstarea unei persoane, de la simptome resimțite la abilitatea de a realiza activități zilnice. Deși este subiectivă, QoL și preferința pacientului sunt aspecte importante de avut în vedere atunci se iau decizii privind tratamentele de administrat.
În afara studiilor clinice, nu trebuie să uităm că ceea ce numim noi “criterii” și “rezultate” sunt lucruri foarte reale care au implicații profunde în viețile oamenilor. De exemplu, pentru pacienții cu cancer mamar avansat, un an în care boala lor nu progresează înseamnă un an în care starea de sănătate nu se deteriorează; un an de “pauză” de cancer. În cazurile cu cancer mamar incipient, dacă un pacient beneficiază de tratament înainte de intervenție chirurgicală și obține pCR, sugerează faptul că tratamentul funcționează. În practică, înțelegerea criteriilor le poate permite pacienților să-și proceseze emoțional diagnosticul
Schimbarea are loc - acum
Pe măsură ce aflăm mai multe despre mecanismele moleculare din spatele diferitelor subtipuri de cancer și sunt introduse din ce în ce mai multe opțiuni terapeutice care prelungesc supraviețuirea, demonstrarea beneficiilor medicamentelor noi în baza standardelor tradiționale devine un lucru dificil de realizat și care consumă timp.
Dovezile care susțin criteriile noi pentru evaluarea medicamentelor oncologice sunt tot mai numeroase, acestea fiind recunoscute din ce în ce mai mult ca o metodă importantă pentru accelerarea procesului de evaluare, păstrând același nivel al calității și garanției asociate în mod tradițional studiilor clinice.

Surse:
1. My Cancer Genome. Molecular Profiling of Lung Cancer. March 2016. Last Accessed 15 September 2016.2. Bosetti C et al. Ann Oncol 2013; 24(10):2657-71.
3. Cancer Research UK. England and Wales Survival (2010-2011) Summary. April 2014. Last accessed 15 September 2016.
4. Verdecchia A et al. Lancet Oncol 2007;8(9):784-96.
5. Pazdur R. Oncologist 2008;13(2):19-21.
6. Johnson JR et al. J Clin Oncol 2003; 21(7):1404-11.
7. http://www.fda.gov; http://www.cancerwatch.com; Johnson JR et al. J Clin Oncol 2003;21:1401-11. Data reflect primary endpoints in pivotal trials of anti-cancer medicines, not including preventative or palliative treatments
8. European Medicines Agency. Appendix 4 to the guideline on the evaluation of anticancer medicinal products in man. December 2015. Last accessed 26 September 2016.
Glosar de termeni:
*PFS Supraviețuirea fără progresia bolii, reprezintă intervalul de timp de la momentul randomizării (includere în studiu clinic) până la progresia bolii sau deces
**ORR reprezintă rata de răspuns obiectiv, respectiv rata totală de răspuns, fie parțial sau complet.
***DFS Supraviețuirea fără semne de boală reprezintă intervalul de timp de la momentul randomizării (includere în studiu clinic) pana la apariţia recurenţei tumorii sau deces